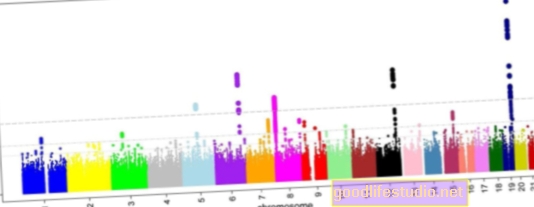
Studiul asupra întregului genom constată mutații ale schizofreniei nedetectate anterior
Un nou studiu, publicat în Comunicări despre natură, sugerează că variantele genetice structurale ultra-rare ar putea juca un rol în schizofrenie.
Majoritatea cercetărilor genetice asupra schizofreniei au încercat să înțeleagă rolul pe care îl joacă genele în dezvoltarea și ereditatea schizofreniei. Și, deși s-au făcut multe descoperiri, încă mai lipsesc multe piese.
Acum, oamenii de știință de la Școala de Medicină a Universității din Carolina de Nord (UNC) au efectuat cel mai mare studiu de secvențiere a genomului întreg asupra schizofreniei, pentru a oferi o imagine mai completă a rolului pe care genomul uman îl joacă în această boală.
Rezultatele noastre sugerează că variantele structurale ultra-rare care afectează limitele unei structuri specifice ale genomului cresc riscul de schizofrenie, a spus autorul senior Jin Szatkiewicz, dr., Profesor asociat în cadrul Departamentului de Genetică al UNC.
Modificările în aceste limite pot duce la dereglarea expresiei genelor și credem că studiile mecanice viitoare ar putea determina efectele funcționale precise pe care aceste variante le au asupra biologiei.
Cercetările anterioare asupra geneticii schizofreniei s-au implicat în principal în utilizarea variațiilor genetice comune cunoscute sub numele de SNP (modificări ale secvențelor genetice comune și care afectează fiecare o singură nucleotidă), variații rare în partea ADN-ului care oferă instrucțiuni pentru fabricarea proteinelor sau variații structurale foarte mari. (modificări care afectează câteva sute de mii de nucleotide).
Aceste studii oferă instantanee ale genomului, deoarece acesta se referă potențial la schizofrenie, dar lasă o mare parte din genom un mister.
În noul studiu, echipa de cercetare a analizat întregul genom folosind o metodă numită secvențierea întregului genom (WGS). Principalul motiv pentru care WGS nu a fost utilizat pe scară largă este că este foarte scump.
Pentru acest studiu, o colaborare internațională a reunit finanțări din subvențiile Institutului Național de Sănătate Mentală și fonduri potrivite de la SciLife Labs din Suedia pentru a efectua secvențierea profundă a genomului întreg la 1.165 de persoane cu schizofrenie și 1.000 de controale - cel mai mare studiu WGS despre schizofrenie cunoscut vreodată.
Ca rezultat, s-au descoperit mutații anterior nedetectabile ale ADN-ului pe care cercetătorii nu le mai văzuseră niciodată în schizofrenie.
În special, descoperirile subliniază rolul pe care domeniile asociate topologic (TAD) (o structură tridimensională a genomului) l-ar putea juca în dezvoltarea schizofreniei. TAD sunt regiuni distincte ale genomului, cu limite stricte între ele, care împiedică domeniile să interacționeze cu materialul genetic din TAD-urile învecinate.
Schimbarea sau ruperea acestor limite permite interacțiuni între gene și elemente de reglare care în mod normal nu ar interacționa.
Atunci când apar aceste interacțiuni, pot exista rezultate negative în expresia genelor care ar putea duce la defecte congenitale, formarea cancerelor și tulburări de dezvoltare.
Cercetătorii au descoperit că variantele structurale extrem de rare care afectează limitele TAD în creier apar semnificativ mai des la persoanele cu schizofrenie decât la cei fără aceasta. Variantele structurale sunt mutații mari care pot implica secvențe genetice lipsă sau duplicate sau secvențe care nu se află în genomul tipic.
Această constatare sugerează că granițele TAD deplasate sau lipsă pot contribui la dezvoltarea schizofreniei, iar variantele structurale care afectează TAD pot fi candidați primari pentru viitoarele studii de schizofrenie.
O posibila investigatie viitoare ar fi sa lucreze cu celule derivate de pacient cu aceste mutatii care afecteaza TADs si sa afle ce s-a intamplat exact la nivel molecular, a spus Szatkiewicz, un profesor asistent adjunct de psihiatrie la UNC.
In viitor, am putea folosi aceste informatii despre efectele TAD pentru a ajuta la dezvoltarea de medicamente sau tratamente de medicina de precizie, care ar putea repara TAD perturbate sau expresii genice afectate, care ar putea imbunatati rezultatele pacientului.
Sursa: University of North Carolina Health Care