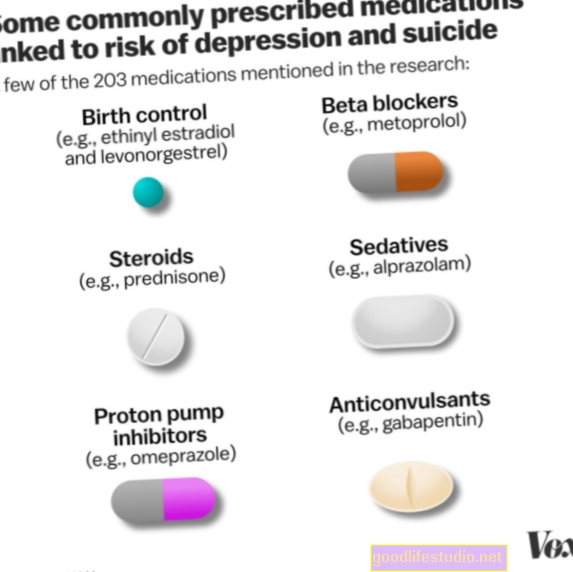
Publicarea Bias din nou, de data aceasta pentru antipsihotice

Antidepresivele au fost deosebit de puternic afectate atunci când se analizează cercetarea pre-aprobare a FDA. De fapt, în recenta lui Lesley Stahl 60 de minute raport despre cercetările antidepresive, s-a îndepărtat complet nedumerită de sensul tuturor. Ce înseamnă atunci când cercetătorii găsesc astfel de descoperiri negative care nu au fost niciodată publicate?
Să aflăm…
În cercetarea actuală, oamenii de știință au examinat 24 de studii pre-comercializare FDA pentru opt antipsihotice de a doua generație (denumite și antipsihotice atipice):
- aripiprazol (Abilify)
- iloperidonă (Fanapt)
- olanzapină (Zyprexa)
- paliperidonă (Invega)
- quetiapină (Seroquel)
- risperidonă (Risperdal)
- injecție cu durată lungă de risperidonă (Consta)
- ziprasidonă (Geodon)
Cercetătorii au comparat apoi rezultatele din documentele de revizuire ale FDA cu rezultatele prezentate în revistele medicale. În mod ideal, s-ar aștepta să găsească 24 de studii publicate, dar în schimb ar putea găsi doar 20:
[… F] testele noastre de premarketing trimise către FDA - care au dat rezultate neplăcute - au rămas nepublicate. Trei au arătat că noile medicamente antipsihotice nu au avut un avantaj semnificativ față de un placebo.
În al patrulea rând, medicamentul a fost superior unui placebo, dar a fost semnificativ inferior unui medicament concurent mult mai puțin costisitor, notează cercetătorii.
Doar 17 la sută din studii nu au fost publicate, ceea ce este de fapt mai mic decât media din industrie pentru aprobările de noi medicamente care își deschid calea prin procesul FDA.
Și acest lucru nu este la fel de rău ca datele - 40 la sută din studii nu au fost niciodată publicate - în jurul antidepresivelor:
În 1998, Moore a folosit Freedom of Information Act pentru a ascunde astfel de date de la FDA. Totalul a ajuns la 47 de studii sponsorizate de companie - pe Prozac, Paxil, Zoloft, Effexor, Serzone și Celexa - pe care Kirsch și colegii le-au analizat apoi. (Ca o parte, s-a dovedit că aproximativ 40 la sută din studiile clinice nu au fost niciodată publicate. Acest lucru este semnificativ mai mare decât pentru alte clase de medicamente, spune Lisa Bero de la Universitatea din California, San Francisco; în general, 22 la sută din studiile clinice studiile cu medicamente nu sunt publicate. „În mare”, spune Kirsch, „studiile nepublicate au fost cele care nu au reușit să arate un beneficiu semnificativ în urma administrării medicamentului propriu-zis”.
În puțin peste jumătate din studiile publicate și nepublicate, el și colegii săi au raportat în 2002 că medicamentul a atenuat depresia nu mai bine decât un placebo. „Și beneficiul suplimentar al antidepresivelor a fost chiar mai mic decât am văzut când am analizat doar studii publicate”, își amintește Kirsch. Aproximativ 82 la sută din răspunsul la antidepresive - nu la 75 la sută pe care le calculase din examinarea numai a studiilor publicate - a fost realizat și de o pastilă falsă.
Important este să țineți cont de faptul că cercetările de pre-comercializare se desfășoară în primul rând pentru a obține un medicament prin procesul FDA. Nu este ultimul cuvânt referitor la eficacitatea unui medicament, este pur și simplu un obstacol birocratic pe care trebuie să îl treacă companiile de medicamente pentru a-și scoate medicamentul pe piață.
Odată lansat pe piață, se efectuează zeci - și în cazul antidepresivelor, sute - de studii suplimentare. Aceste studii, care sunt adesea mai variate, independente și realizate de o gamă mai largă de cercetători, constituie în cele din urmă majoritatea cercetărilor privind eficacitatea unui medicament.
Deci, linia de argint a acestei ultime cercetări este că procentul de studii publicate niciodată nu este de fapt inferior decât media industriei și semnificativ mai mic decât numărul de studii publicate niciodată înainte de aprobarea antidepresivelor.
Referinţă
Turner, E.H., Knoepflmacher, D. și Shapley, L. (2012). Publicarea Bias în testele antipsihotice: o analiză a eficacității comparând literatura publicată cu baza de date a SUA Food and Drug Administration. Medicina PLoS, 9 (3): e1001189. doi: 10.1371 / journal.pmed.1001189